Vaccine Nanocovax chưa được thông qua cấp phép
Bộ Y tế đã họp vào ngày hôm qua (29/8/2021) nhằm xem xét về việc việc cấp phép khẩn cấp cho vaccine Nanocovax. Theo đó, nhóm nghiên cứu được đề nghị tiếp tục bổ sung hồ sơ vaccine Covid-19 Nanocovax.
Theo thông cáo báo chí, Hội đồng tư vấn đã thẩm định hồ sơ vaccine Nanocovax kỹ lưỡng, nhiều lần, dựa trên hồ sơ pháp lý, chất lượng, dược lý, lâm sàng và kết luận của Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia (Hội đồng đạo đức).
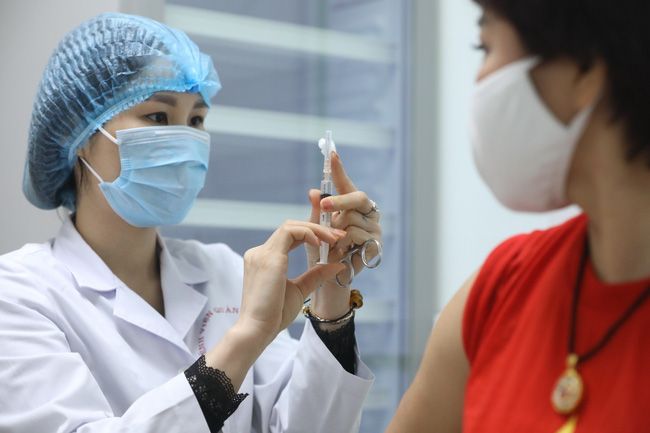
Đã có trên 13.000 người thử nghiệm tiêm vaccine Nanocovax
Sau buổi họp, Hội đồng tư vấn ghi nhận các kết quả đạt được đối với hồ sơ đề nghị cấp giấy đăng ký lưu hành vaccine Nanocovax. Hội đồng tư vấn đề nghị doanh nghiệp tiếp tục bổ sung: Hồ sơ chất lượng; Hồ sơ dược lý, lâm sàng bổ sung tính an toàn của toàn bộ người đã được tiêm ít nhất một liều vaccine tới hiện tại và giải thích rõ về các trường hợp gặp phản ứng nghiêm trọng (SAE).
Theo đó, Hội đồng tư vấn tiếp tục đề nghị Công ty Nanogen khẩn trương bổ sung, cập nhật các nội dung trên. Sau đó, công ty phải báo cáo Hội đồng Đạo đức và Hội đồng tư vấn tiếp tục xem xét, thẩm định cuốn chiếu các kết quả nghiên cứu để cấp phép khẩn cấp.
Theo quy trình, sau khi thông qua hồ sơ, Hội đồng tư vấn sẽ đề xuất Bộ Y tế cấp phép khẩn cấp cho vaccine. Như vậy, sau cuộc họp hôm 29/8/2021, Hội đồng tư vấn đề nghị doanh nghiệp bổ sung hồ sơ, có nghĩa chưa tiến tới bước đề xuất cấp phép cho Nanocovax.
Sau khi doanh nghiệp khẩn trương bổ sung, cập nhật các nội dung nêu trên, báo cáo Hội đồng Đạo đức và Hội đồng Tư vấn tiếp tục xem xét, thẩm định cuốn chiếu các kết quả nghiên cứu để có thể cấp giấy đăng ký lưu hành có điều kiện trong trường hợp cấp bách.
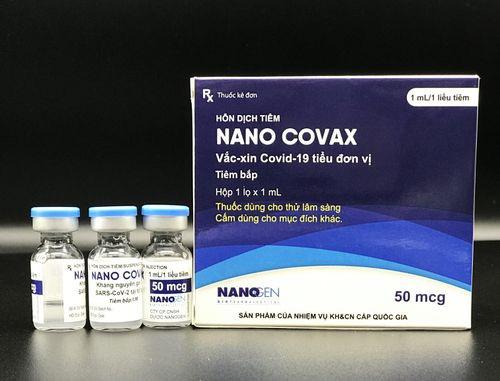
Đến thời điểm hiện tại, Nanocovax của Công ty Nanogen là vaccine COVID-19 đầu tiên của Việt Nam triển khai thử nghiệm lâm sàng (TNLS) thứ 3, với 13.000 người tham gia, độ tuổi từ 18, bao gồm nhóm người cao tuổi, người có bệnh nền.
Pha 3 đã được thử nghiệm trên 13.000 người, chia làm 2 giai đoạn nhỏ (3a: 1.000 người và 3b: 12.000 người).
Theo nhóm nghiên cứu, vaccine Nanocovax đạt yêu cầu về tính an toàn và tính sinh miễn dịch.
Nanocovax đang thử nghiệm giai đoạn 3b. Giai đoạn 3a đang được đánh giá tính sinh miễn dịch vào ngày thứ 42 sau tiêm liều một, dự kiến đến ngày 10/9 hoàn thành.
Lê Quốc





 In bài viết
In bài viết








